Измерение теплофизических свойств веществ и материалов
Методы и средства измерений и контроля теплофизических свойств веществ и материалов
Теплофизические свойства принято подразделять на несколько групп. Первую группу составляют равновесные теплофизические свойства веществ, являющиеся функциями состояния. К этой группе относятся так называемые термодинамические свойства, которые, в свою очередь, подразделяются на термические и калорические. К термическим свойствам относятся плотность вещества, к калорическим свойствам относят внутреннюю энергию, энтальпию, энтропию, теплоемкость.
Ко второй группе теплофизических свойств веществ относят «переносные» свойства, такие как теплопроводность, вязкость, диффузия. Эти свойства характеризуют неравновесные процессы в физических средах. К теплофизическим свойствам относятся также некоторые оптические свойства, связанные с поглощением и испусканием теплового излучения.
Рассмотрим некоторые теплофизические свойства веществ и материалов, методы и средства их измерения и контроля.
Единицей количества теплоты Q является джоуль (Дж). Джоуль — это количество теплоты, эквивалентное механической работе (энергии) 1 Дж. В технике пока еще нередко применяется старая (внесистемная) единица количества теплоты — калория (кал). Соотношение между ними:
1 кал = 4,1868 Дж;
1 Дж = 1 Вт*с = 1 Н*м.
Тепловой поток Ф — это количество теплоты, проходящей через поперечное сечение за единицу времени Г:
Ф = ΔQ/ ΔT.
Тепловой поток измеряется в единицах мощности (Дж/с), которые могут быть переведены в другие единицы мощности:
1 Дж/с = 1 Вт = 1 Н*м/с.
Для грубых практических расчетов можно принимать
1 ккал/ч = 1 Вт.
Теплоемкость вещества С (ранее называвшаяся также водяным эквивалентом) означает изменение теплосодержания вещества (энтальпии) при изменении его температуры на 1 К:
C = ΔQ/ΔV.
Единицей измерения теплоемкости является джоуль на кельвин; 1Дж*К-1 — это теплоемкость тела, температура которого повышается на 1К при подведении к нему количества теплоты 1Дж.
Напомним, что кельвин (К) — это 1/273,16 части термодинамической температуры тройной точки воды.
Удельная теплоемкость вещества — это величина, равная количеству теплоты, необходимой для нагревания 1 кг вещества на 1К.
Единица удельной теплоемкости — джоуль на килограмм-кельвин (Дж/(кг*К)).
Вблизи нуля Кельвина теплоемкость тел пропорциональна T3.
Алмаз, например, имеет теплоемкость, равную 3R при 1800 К.
Если в одной области вещества (газа, жидкости, твердого тела) энергия молекул больше, чем в другой, то с течением времени вследствие постоянных столкновений молекул происходит процесс выравнивания средних кинетических энергий молекул, иными словами, выравнивание температур. Изменение температуры в пространстве характеризуется градиентом температуры.
Передача теплоты вследствие наличия такого свойства вещества, как теплопроводность, всегда происходит в направлении уменьшения температуры.
Теплопроводность — градиент температуры, равный скорости изменения температуры на единицу длины в направлении нормали к этой площадке.
Теплопроводность численно равна плотности теплового потока при градиенте температуры, равном единице.
Важными величинами теплофизических свойств веществ и материалов являются температурные коэффициенты линейного и объемного расширения.
Температурный коэффициент линейного расширения a1 — это изменение тела длиной в 1 м при изменении его температуры на 1К. Единица измерения— метр на метр-кельвин (м/(м*К)).
Температурный коэффициент объемного расширения av — это изменение объема тела (вещества) в 1м3 при изменении его температуры на 1К. Единица измерения — кубический метр на кубический метр-кельвин (м3/(м3*К)).
Явление диффузии заключается в том, что происходит самопроизвольное проникновение и перемешивание двух соприкасающихся газов, жидкостей и твердых тел. Диффузия сводится к обмену масс частиц этих тел; она возникает и продолжается, пока существует градиент плотности.
Методы и средства измерений и контроля теплофизических свойств веществ и материалов довольно разнообразны.
Рассмотрим принцип действия основного средства измерений теплофизических свойств веществ и материалов — калориметра.
Калориметр обычно работает таким образом, что после инициирования какого-либо процесса проба (образец) отдает калориметрическому устройству или получает от него некоторое неизвестное количество теплоты ΔQ. При этом специальными мероприятиями предотвращается теплообмен калориметрического устройства с окружающей средой. В соответствии с изменением энтальпии калориметра на ΔQ его температура повышается или понижается на ΔT. Это изменение температуры и является мерой количества теплоты ΔQ, участвовавшей в теплообмене. Таким образом, измерение количества теплоты сводится к определению разности температур.
На этом принципе построены калориметры для измерения теплоемкости, теплопроводности, коэффициентов теплопередачи и других теплофизических свойств веществ. Рассмотрим некоторые из них.
Теплоемкость твердых тел обычно исследуют как функцию температуры при давлении, равном атмосферному.
Метод непосредственного нагревания заключается в следующем. На исследуемом образце 5 (рис. 2.99, а) намотан электрический нагреватель 4. Образец помещен в цилиндр 3 из того же материала. Нагреватель одновременно служит термометром сопротивления. Образец подвешивается внутри сосуда 2, соединенного с вакуумной линией 1. Калориметр помещается в криостат, где создается стационарная температура.
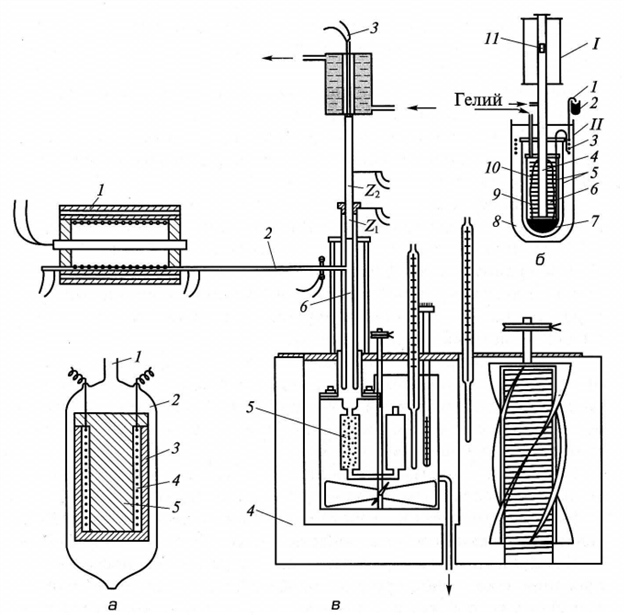
Рис. 2.99. Измерение теплоемкости веществ и материалов:
а — конструкция калориметра непосредственного нагревания: 1 — вакуумная линия; 2 — сосуд; 3 — цилиндр; 4 — электрический нагреватель; 5 — исследуемый образец; б — конструкция ледяного калориметра: 1 — капилляр для подачи ртути; 2 — сосуд; 3 — термостатирующая спираль; 4 — приемный канал калориметра; 5 — калориметр; 6 — лед; 7 — ртуть; 8 — тающий лед; 9 — вода; 10 — металлические ребра; 11 — ампула с исследуемым веществом; I — электрод, II — ледяной калориметр; в — конструкция калориметра смешения: 1 — печь; 2— трубка; 3 — термопара; 4 — термостат; 5 — калориметр; 6 — платиновый нагреватель
Измерив разность температур образца до и после включения нагревателя, определив количество теплоты, подведенное к измеряемому образцу за счет работы нагревателя, определяют теплоемкость образца.
Метод смешения заключается в том, что в печи образец нагревается до нужной температуры, после чего его сбрасывают в расположенный под печью калориметр, в котором он остывает до температуры, близкой к комнатной. В калориметре измеряется теплота, отданная образцом при его остывании.
Ледяной калориметр (рис. 2.99, б) позволяет определить количество теплоты жидкого вещества с высокой точностью. Нагретую в электропечи до определенной температуры ампулу с исследуемым веществом 11 сбрасывают в ледяной калориметр II. Количество теплоты, введенное с ампулой в калориметр, определяется по массе расплавившегося льда б, намороженного на металлических ребрах 10, и теплоте плавления льда. Массу определяют по уменьшению объема системы лед 6 — вода 9 в калориметре 5, а это изменение объема определяют по количеству ртути 7, втянутой внутрь калориметра по приемному каналу калориметра 4 по капилляру для подачи ртути 1 при плавлении льда. Количество ртути 7 находят весовым методом по ее убыли в сосуде 2. Калориметр 5 окружен тающим льдом 8 для исключения притока теплоты извне.
Метод смешения часто применяют для определения теплоемкости газа. Конструкция калориметра смешения для измерения теплоемкости газов представлена на рис. 2.99, в. Исследуемый газ предварительно подогревается в печи 1. Затем он поступает по трубке 2 в основной платиновый нагреватель б, состоящий из двух концентрично расположенных платиновых трубок, по которым пропускается электрический ток через токопроводы Z, и Z2. Температура газа, покидающего печь и поступающего в калориметр 5, измеряется термопарой 3, расположенной внутри основного нагревателя. Калориметр 5 окружен калориметрической жидкостью термостата 4, которая непрерывно перемешивается. Повышение температуры калориметра измеряется термометрами. Исследуемый газ, выходящий из калориметра, охлаждается до температуры калориметра.
Для определения теплопроводности веществ используют две группы методов: стационарные и нестационарные. В нестационарных методах в отличие от стационарных применяют изменяющиеся по определенному закону во времени температурные поля.
Один из методов определения теплопроводности металлов, нашедший широкое применение, является метод продольного теплового потока.
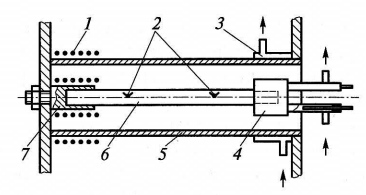
Рис. 2.100. Конструкция установки для измерения теплопроводности металлов методом продольного теплового потока:
1 — нагреватель охранного цилиндра; 8 — термопары; 3 и 4 — холодильники; 5 — охранный цилиндр; 6 — образец; 7 — блок нагревателя
На рис. 2.100 изображена конструкция установки, построенная на этом методе. Вдоль длинного образца 6 с заданной площадью поперечного сечения создается равномерный тепловой поток с помощью блока нагревателя 7 или холодильника 4. Между двумя сечениями образца, расположенными на определенном расстоянии, измеряют с помощью термопар 2 разность температур. Защита образца от боковых тепловых потерь осуществляется с помощью охранного цилиндра 5, в котором создается температурное поле, повторяющее поле образца с помощью нагревателя охранного цилиндра 1 или холодильника 3. По измеренной разности температур определяют теплопроводность образца.
Для определения теплоты сгорания твердых, жидких и газообразных веществ, применяемых в теплосиловом хозяйстве, используют калориметры горения.
Известно, что при полном сгорании вещества выделяется некоторое количества теплоты О (теплота сгорания). Если разделить ее на массу т (или объем при нормальных условиях Vn), то получится (удельная) теплота сгорания:
Н= Q/т (Дж/кг)
или
Hn = Q/Vn( Дж/м3).
Этот показатель нужен для определения коэффициентов полезного действия, расчетов экономности и расхода энергии в различных установках, а также для оптимального управления процессом горения.
Для быстро протекающих процессов горения твердых и жидких веществ разработана так называемая калориметрическая бомба Бертло (рис. 2.101). Сжигание малого, точно отмеренного количества вещества 4 происходит при постоянном объеме в герметической емкости в атмосфере возможно более чистого кислорода под давлением ~ 3 МПа (30 ат). Заполненная емкость помещается в жидкостную ванну калориметра, которая и воспринимает выделяющееся тепло горения.
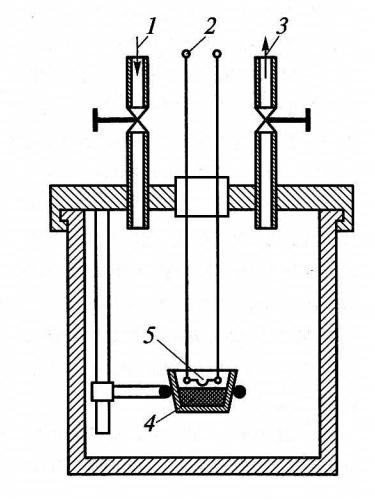
Рис. 2.101. Устройство калориметрической бомбы Бертло:
1 — клапан для подачи кислорода; 2 — запальное напряжение; 3 — клапан для отвода продуктов сгорания; 4 — исследуемое вещество; 5 — электрический запальник
Исследуемое вещество 4 помещают в чашечки из платины или кварца или в малые пластмассовые капсулы. На крышке, закрепляемой к корпусу емкости, расположены устройства, необходимые для измерения: клапаны для подачи кислорода 1 и отвода продуктов сгорания 3, держатели для проб и электрический запальник 5. Зажигание осуществляется подводом электричества к тонкой платиновой проволоке, причем подводимое для зажигания тепло также должно быть точно измерено для учета при определении теплоты сгорания вещества.
Твердые вещества обычно прессуют в брикеты (таблетки) малых размеров и взвешивают с высокой точностью. Плохо горящие вещества перемешивают с хорошо горящими жидкостями с известной теплотой сгорания.
При определении теплоты сгорания в калориметрической бомбе измеряют количество воды, образующейся при химических реакциях и находящейся в парообразном состоянии в продуктах сгорания.
Достижимая точность теплообменных калориметров сравнительно высокая. Их погрешность не превышает ±(0,25... 1) %. Сухие калориметры имеют погрешность от +(1 ...2) % верхнего предела диапазона измерений.
| Температура. Измерение и контроль температуры. Методы и средства измерения температуры. |
| Волнистость и шероховатость. Измерение и контроль волнистости и шероховатости |
| Поверочные линейки и плиты |

